2020.4.2
“スライムの化学”で難題を克服! 次世代がん治療法の効果を最大化する魔法の材料とは
東京工業大学 科学技術創成研究院 化学生命科学研究所 西山研究室 助教 野本貴大【前編】
ことし1月に発表されたある研究成果が一大ニュースとして注目を浴びた。それは、“液体のりでがん治療効果が劇的に向上する”という衝撃的なものだった。一見、何の関係もなさそうに思える液体のりが、どのようにがん治療に関係してくるのか。そのメカニズムとは何なのか──。同研究を中心となって推し進めた東京工業大学 野本貴大助教に話を聞いた。
中性子のエネルギーと薬剤でがん細胞をやっつける
厚生労働省が2019年に発表した人口動態統計によれば、2018年にがんで亡くなった日本人は37万3584人。これは、実に死亡総数の約3割の人ががんで亡くなっている計算で、1981(昭和56)年以降、36年連続で死因のトップになる結果となった。日本人の生命を脅かす大きな敵と言っても決して過言ではない存在が「がん」なのだ。
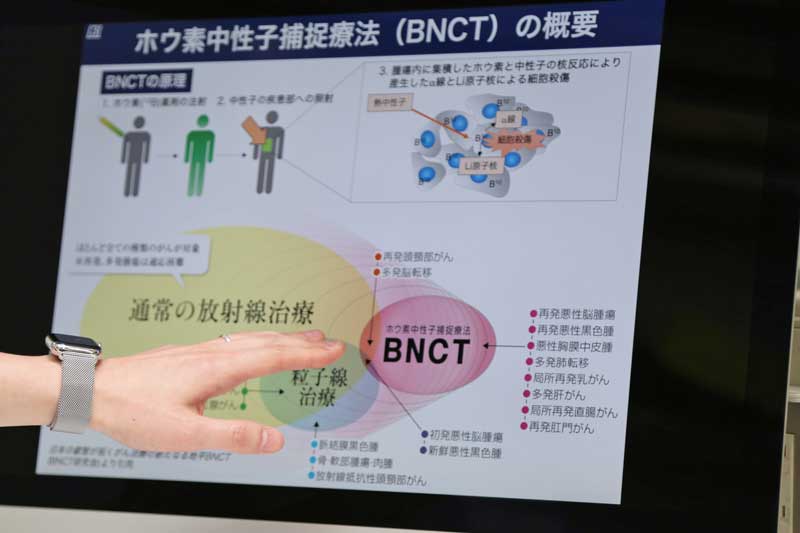
日本はもちろん世界中でがん治療の研究が進められる中で、ことし1月に日本の研究グループが行った発表により、ホウ素中性子捕捉療法(Boron Neutron Capture Therapy、以下BNCT)と呼ばれるアプローチが新たながん治療法として脚光を浴びている。
「BNCTは意外に歴史が古く、米国では1950年代から研究されてきたのですが、当時は薬剤や中性子線の質が悪く、臨床試験で良い結果を得られませんでした。しかし、日本ではこつこつと研究が重ねられ、2000年代になってついに花が開き始めました。この領域では今、日本が断トツで世界をリードしているんですよ」
こう語るのは、東京工業大学でがん治療を研究する野本貴大助教。今回、話を伺うキッカケとなった“液体のりの成分ががん治療に役立つメカニズム”を突き止めた若きトップランナーだ。

-
次世代のがん治療法として期待されている、BNCTの効果を最大化する可能性を見いだした野本助教
野本助教の専門分野は薬物送達学。
これは、治療に必要な薬物を、特定の細胞だけに“選択的に届ける”方法を研究する学問だ。カプセル化した抗がん剤を特定の場所に届けるナノマシンなど、現在さまざまな医療分野での利用が期待されており、BNCTもその一つとなっている。
がん治療には、外科治療、薬物療法(抗がん剤治療)、放射線治療という3つの標準的な治療法がある。これらに加えて、人体が持っている免疫本来の力を高める「免疫療法」が第4のがん治療法として近年注目を集めている。そして今、第5の治療法として期待されているのが、光や中性子などの物理エネルギーと薬物を組み合わせるBNCTのような治療法だ。
先ごろ、3月25日に薬剤が承認されたことが発表され、期待はさらに高まっている。
「BNCTは、体内に入れたホウ素化合物(BPA)に中性子線を照射することで起きる核反応を利用し、がん細胞を死滅させようという治療法です。ホウ素化合物は人体への影響がほとんどなく、治療に使われる熱中性子もエネルギー自体はとても低いため、単体で使っても効果はありません。ところが、この2つを組み合わせると核反応を起こし、アルファ粒子とリチウム反跳(はんちょう)核による高いエネルギーが生じて、がん細胞に強いダメージを与えるのです」

-
薬物療法と放射線治療を掛け合わせた第5のがん治療法BNCT。がん細胞の殺傷効果が高く、健康な細胞への影響が少ないと期待される
ホウ素化合物と熱中性子の核反応で生じるエネルギー量はとても大きく、がん細胞を十分に殺傷する能力がある。
その一方で、アルファ粒子とリチウム反跳核の移動距離はとても短く、わずか“細胞1個分(10マイクロメートル以下)”しかない。
そのため、選択的にがん細胞だけを攻撃することが可能になり、健康な器官への影響が極めて少ない治療法なのだ。
がん細胞の貪欲さを逆手にとった戦術
ホウ素化合物は、体内に入るとがん細胞だけに集積していくという特徴を持っている。現在、臨床試験で使われているホウ素化合物はボロノフェニルアラニンという物質で、必須アミノ酸であるフェニルアラニンにホウ素を付加したもの。がん細胞はこれを栄養分と認識し、LAT1というアミノ酸トランスポーターを介して細胞内に取り込むのだという。
そう聞けば、がん細胞だけに薬物を届ける理想的なメカニズムに思えるが、実はある課題を抱えていた。
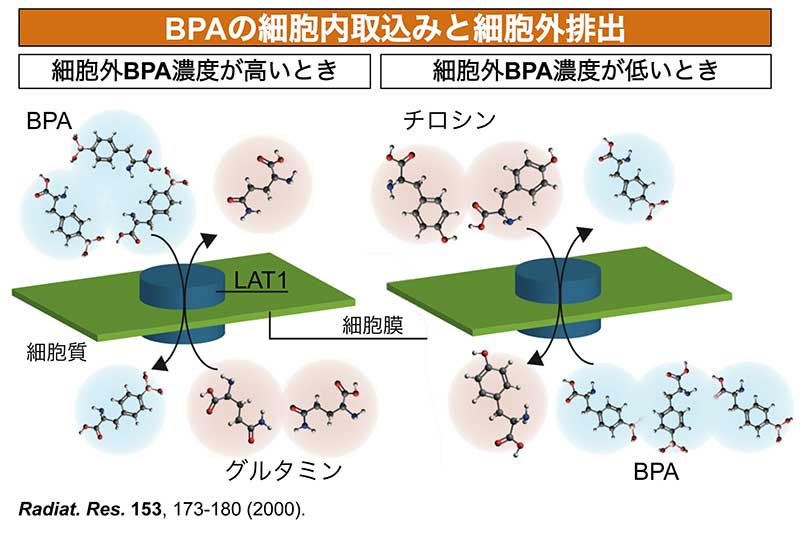
「LAT1というトランスポーターは、がん細胞にとって“口”のようなもの。最初はそこからBPAをぱくぱく食べてくれるのですが、細胞外のBPAが少なくなってくると、代わりに別のアミノ酸を食べ始め、細胞内のBPAを吐き出してしまいます。するとBPAは細胞の中に長くとどまることができないため、治療効果が著しく落ちてしまうのです。それが従来のホウ素化合物が持つ大きな弱点でした」

-
細胞外のBPA濃度が高いときはBPAをがん細胞内に取り込む(左)が、細胞外のBPA濃度が低下するとがん細胞外へBPAを排出し、代わりにアミノ酸を取り込む(右)
最初に食べていたエサが少なくなってきたと知るやいなや、他のエサに乗り換え、元のエサを吐き出す──。
がん細胞が持つこの厄介な特性に対応するためにも、ホウ素化合物の滞留性を上げることが、BNCTの治療効果を高める上で重要だった。
そこで野本助教が思い付いたのが、通常の分子よりも大きな「高分子」に、薬剤であるホウ素をくっつけるという方法。より大きな分子ならLAT1が口を広げても、そのままのみ込むことはできない。ではそのとき、がん細胞がどのような行動をとるのだろうか?
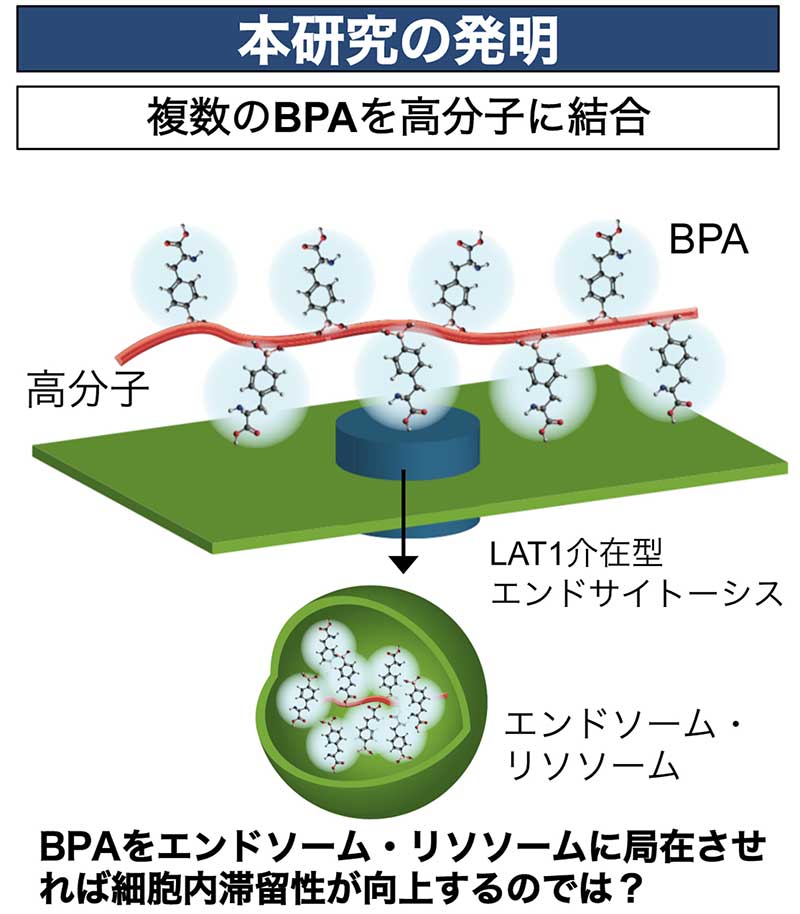
野本助教は、薬剤をくわえたまま細胞膜ごと形を変えてボール状に包み込み、取り込んでしまうのだと教えてくれた。これは「エンドサイトーシス」と呼ばれる現象で、そこでできた小胞を「エンドソーム・リソソーム」という。
要は、取り込まれた薬剤が通常の細胞質とは別の空間に隔離されるため、吐き出されにくくなるだろう、と野本助教は考えたのだ。

-
BPAを高分子と結合させることでがん細胞内への取り込み方(エンドサイトーシス)が変わり、エンドソーム・リソソームという小胞内に薬剤がとどまる
「高分子に何を使おうか? というときに注目したのが、液体のりの主成分であるポリビニルアルコールでした。この物質を選んだ理由の一つは、ホウ素との相性がすごく良くて、水の中で混ぜるだけで簡単に反応してくれるからです」

-
野本助教が見せてくれた、高分子ポリビニルアルコールの粉末。ホウ素化合物と液体のりの主成分であるポリビニルアルコールを水の中で混ぜることで簡単に結合するという
実はこれ、小学生でもできる化学実験として知られる「スライムの化学」と同じ原理。
スライムを作るときにはポリビニルアルコールが主成分である洗濯のりと、ホウ砂(ほうしゃ・四ホウ酸ナトリウム)を使用する。
ホウ砂を水中で溶かすとホウ酸イオンが生成され、複数のポリビニルアルコールをつないでゲル化(架橋)し、スライムができあがるというものだ。

-
水酸基OHが連なるシンプルな構造を持ったポリビニルアルコールは、ホウ素化合物と結合しやすい性質を持つ
ちなみに、今回発見したホウ素化合物とポリビニルアルコールを結合させたものは、当然ながらスライムや液体のりのようにはゲル化しない。ホウ砂とは構造が異なり、BPAが一つのポリビニルアルコール分子に結合するだけで、複数の高分子をつなぐことはないためだ。液体であるため、従来の薬剤と同じように注射で体内に入れることができる。
「ポリビニルアルコールの構造はとてもシンプルで、BPAと結合しても必須アミノ酸であるフェニルアラニンの構造はそのままです。これが、がん細胞に食べられやすい状態を保ってくれるのです」
将来的な普及も視野に入れた上での選択
ポリビニルアルコールを起用した理由は他にもある。
液体のりや洗濯のりといった身近な日用品の主成分となっていることからも分かるように、人体への適合性が高く、悪影響が少ないからだ。
「BNCTは薬剤の投与量がとても多く、体重1kgに対して500mgの薬剤を投与する必要があると言われています。体重60kgの人なら30g。これは、薬剤としてはかなりの量です。それだけ多くの量を体内に入れるのですから、安全であるに越したことはありません。その点、ポリビニルアルコールは古くから使われている物質で、安全性については十分に確かめられています」

-
将来、どんな場所でも作ることができる実現可能性の高さも視野に入れて、最適な構造の高分子を探し求めたという野本助教
さらにコストの安さもポイントだった。
もちろん同じポリビニルアルコールでもBNCTで使用するのは、液体のりなどの日用品とは異なり、医薬品専門メーカーが製造するもの。それでも他の医薬品材料に比べると圧倒的な価格差がある。将来、この治療法が承認された後に、より多くの人が利用できるよう、高価な材料は使いたくないというのが野本助教の思いだ。
後編では、新たな薬剤によってどのような治療効果が得られるのか。また、野本助教が今回の大発見に至った思考方法に迫っていく。
<2020年4月3日(金)配信の【後編】に続く>
投与から数時間を経ても薬剤の効果が持続! さらにはあらゆる部位のがんに適用できる可能性も

-
この記事が気に入ったら
いいね!しよう -
Twitterでフォローしよう
Follow @emira_edit
text:田端邦彦 photo:安藤康之